El cáncer de colon [1] es una de las principales causas de cáncer a nivel global, tanto en mujeres (segunda causa tras el cáncer de mama) como en hombres (tercera, tras los cánceres de próstata y de pulmón). En España, el cáncer de colon es la segunda causa de muerte por tumores, sólo detrás del cáncer de pulmón. Es especialmente prevalente en personas de más de 65 años, lo que lo hace especialmente preocupante dada la tendencia al envejecimiento de la población en los países desarrollados.
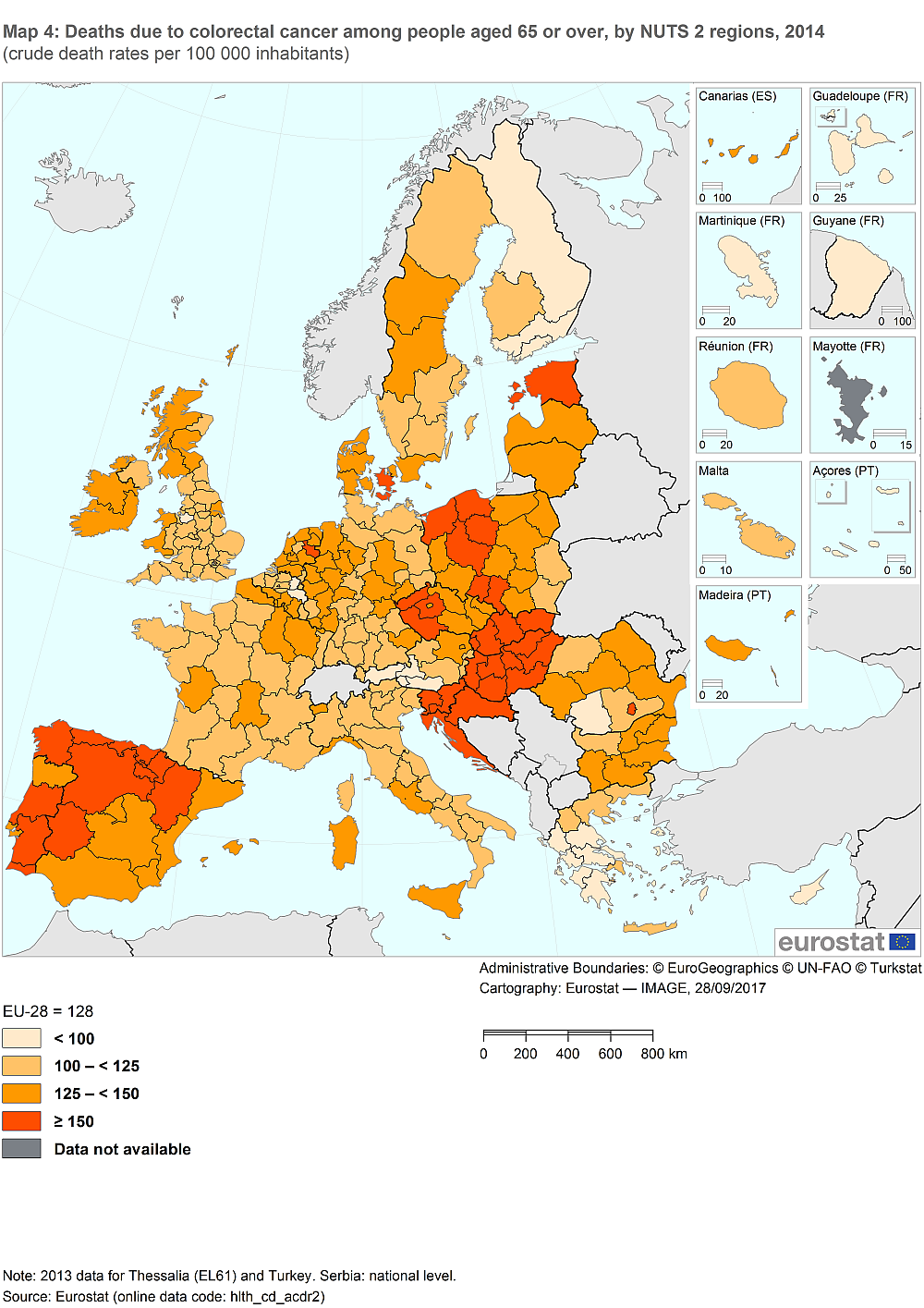
En la actualidad, las dos mejores herramientas de las que disponemos contra el cáncer de colon son la prevención y la detección precoz. Sólo alrededor del 5% de los casos diagnosticados de cáncer de colon se pueden asociar directamente a factores genéticos, siendo sus auténticos factores de riesgo la inadecuada alimentación, obesidad, ingesta de alcohol, ser fumador y la falta de actividad física, lo que ha llevado a algunos expertos a calificar al cáncer de colon como “una enfermedad de nuestra civilización”[3]. Afortunadamente, un estilo de vida saludable puede ayudarnos a reducir enormemente el riesgo de padecer cáncer de colon. No menos importante es la detección precoz de los tumores. Con un sencillo análisis de sangre oculta en las heces, se pueden detectar estos tumores hasta 10 años antes de volverse malignos. Se estima que el 90% de los casos de cáncer de colon detectados precozmente pueden curarse con éxito, mediante procedimientos más sencillos, y con menor riesgo de reincidencia.Dada la especial relevancia de esta variedad de cáncer, en la actualidad se están desarrollando diversas líneas de investigación relacionadas con el cáncer de colon. Desde el cultivo y el estudio en el laboratorio de las células individuales que forman parte de un tumor, hasta las pruebas clínicas de nuevos fármacos en pacientes con este tipo de cáncer, pasando por la investigación en modelos animales de la enfermedad. Todos estos enfoques presentan claras ventajas, como la versatilidad y simplicidad de los modelos celulares, el estudio in situ de los tumores en los estudios con pacientes y la posibilidad de realizar pruebas invasivas con los modelos animales. Sin embargo, estos planteamientos presentan también claras desventajas: los modelos celulares no se encuentran necesariamente el mismo entorno que las células cancerosas, los modelos animales de esta enfermedad no tienen por qué comportarse y responder como los humanos, y las pruebas con pacientes humanos son necesariamente lentas y se realizan con limitaciones debido a las estrictas normas de seguridad.
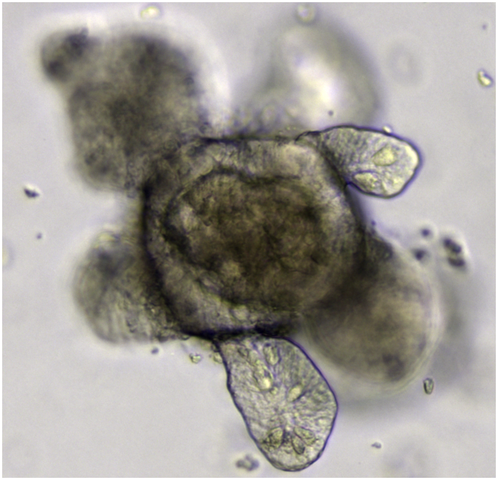
En la actualidad, se comienza a emplear una técnica innovadora en la investigación biomédica, especialmente relevante para el estudio del cáncer, llamada “Organoides” [4]. Un organoide es una estructura tridimensional en miniatura, producida in vitro, y que captura características anatómicas y funcionales de un órgano. Generalmente se forman a partir de una o unas pocas células madre (sanas o tumorales) que se auto-organizan en un cultivo estable, capaz de mostrar algunas de las funciones del órgano simulado.
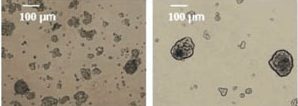
Las suspensiones celulares forman pequeños grupos de células 1 semana después de la siembra (arriba a la izquierda). Después de 10 pases, el 1% de las esferas persisten como esferoides prototípicos (arriba a la derecha). Fuente: By Chang, H.L., MacLaughlin, D.T., and Donahoe, P.K., Somatic stem cells of the ovary and their relationship to human ovarian cancers (April 30, 2009), StemBook, ed. The Stem Cell Research Community, StemBook [CC BY 3.0 (http://creativecommons.org/licenses/by/3.0)], via Wikimedia Commons
[1] Cáncer colorectal, Wikipedia
[2] http://ec.europa.eu/eurostat/statistics-explained/index.php/Causes_of_death_statistics_-_people_over_65
[3] Colon cancer, a civilization disorder. Watson A. J. and Collins P. D. Digestive diseases, 29(2), 222-228. (2011).
[4] https://en.wikipedia.org/wiki/Organoid
[5] Engineered cardiac organoid chambers: toward a functional biological model ventricle. Lee, E. J. et al. Tissue Engineering Part A, 14(2), 215-225. (2008).
[6] Mammary organoids from immature virgin rats undergo ductal and alveolar morphogenesis when grown within a reconstituted basement membrane. Darcy, K. M. et al. Experimental cell research, 196(1), 49-65. (1991).
Autor: Manuel Gómez, investigador postdoctoral
grupo Integrative Cell and Tissue Dynamics del IBEC